Первая часть находится здесь
Мы пойдем другим путем!
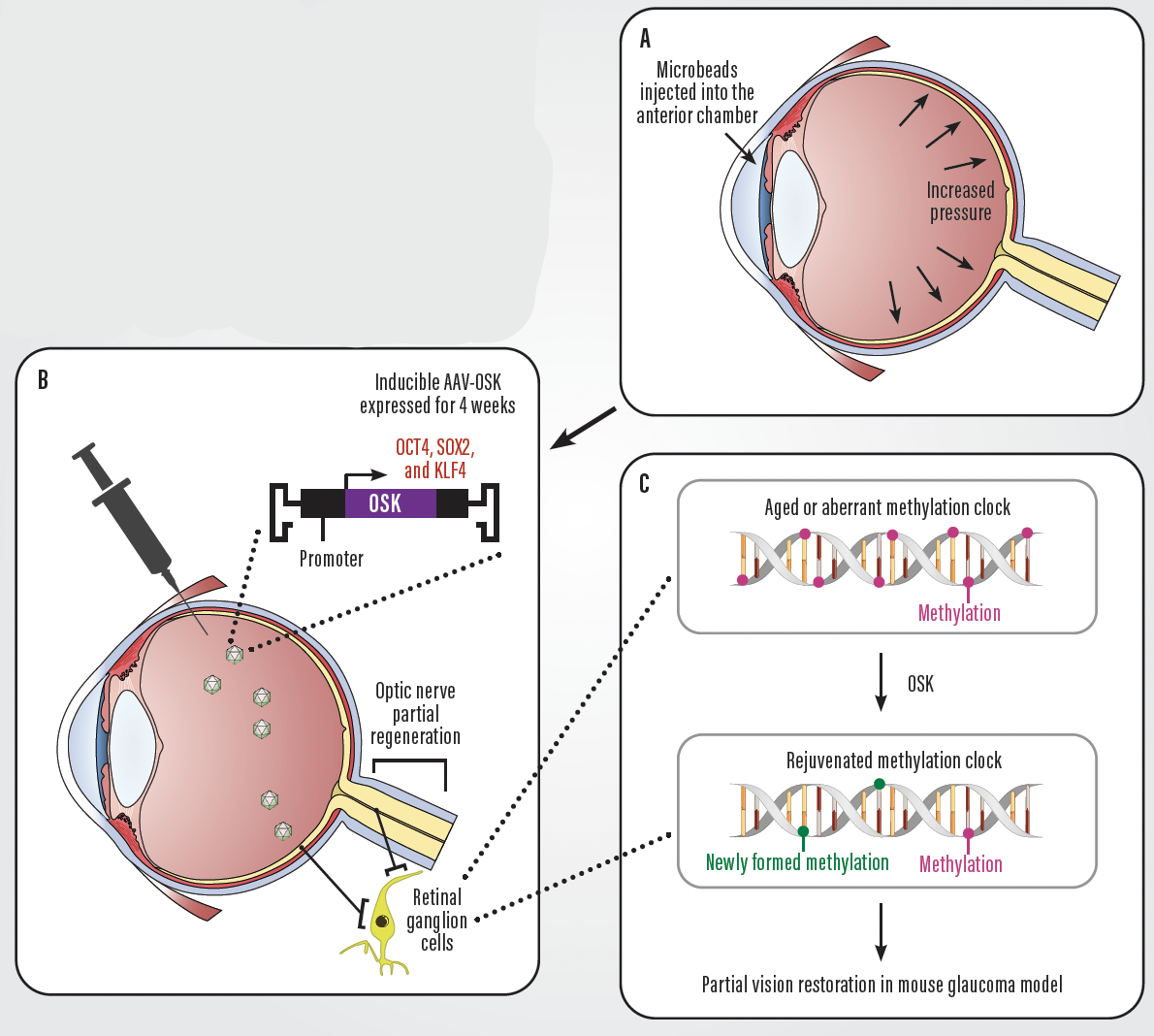
Несколько лет назад в лаборатории Гарвардского университета учёные сжали зрительные нервы здоровых мышей, чтобы вызвать состояние, похожее на инсульт глаза.
Затем в глаза грызунам ввели вирус, содержащий три фактора Яманаки.
«Вот тут-то Дэвид Синклер и пришел с блестящей идеей. Он показал, что, если использовать всего три из этих факторов — Oct4, SOX2 и KLF4, или OSK, как мы его называем, — можно продолжать давать их в течение длительного времени без риска. И самое крутое, что клетки сохраняют свою идентичность. Клетка легкого остается клеткой легкого, клетка сердца остается клеткой сердца. А в нашем случае ганглиозная клетка сетчатки остается ганглиозной клеткой сетчатки. Когда мы увидели, какие терапевтические преимущества это может иметь, мы поняли, что наткнулись на что-то большое», - рассказала Шарон Розенцвейг-Липсон, главный научный сотрудник Life Biosciences.
Кроме того, эти факторы были «запрограммированы» на активацию только в присутствии антибиотика доксциклина. Исследователи по графику давали мышам воду с антибиотиком (два дня с ним, пять дней без) в течение двух месяцев.
Идея заключалась в том, чтобы перепрограммировать клетки лишь частично: убрать большую часть метильных меток, но не все, чтобы клетки не утратили свою функцию, а просто «помолодели» и лучше справлялись с лечением.
Такая схема позволяла избежать тератом. Клетки не превращались полностью в стволовые, а оставались собой, только моложе.
Другие компании и исследователи идут другими путями. Например, компания Altos Labs (ее консультирует сам Яманака), изучает, как технологии перепрограммирования могут омолаживать ткани и органы, не вызывая плюрипотентности, путем тонкой настройки процесса перепрограммирования. Это означает сброс клеток в более молодое, здоровое состояние с сохранением их специализированных функций.
Вместо полного перепрограммирования клеток, подход Altos Labs фокусируется на частичном и контролируемом перепрограммировании, который сбрасывает биологические часы, не дестабилизируя клетку.
Все ближе к испытаниям на людях

В декабре 2020 года журнал Nature опубликовал результаты эксперимента гарвардских ученых под названием «Поворот времени вспять?» Исследователям удалось не только зафиксировать омоложение клеток на эпигенетическом уровне, но и добиться регенерации поврежденных зрительных нервов у подопытных грызунов. Страшного побочного эффекта в виде тератом удалось избежать.
«Это было довольно захватывающе», - сказал Дэвид Синклер, генетик из Гарварда, старший автор исследования на мышах.
Коммерческий потенциал технологии быстро оценили в биотехе - уже в 2021 году разработка Синклера была лицензирована компанией Life Biosciences.
Два года спустя компания отчиталась об успешном повторении эксперимента на приматах. У обезьян с травмами зрительного нерва наблюдалось частичное восстановление зрения при отсутствии опухолевых процессов. Правда, полноценная научная публикация этих данных пока ожидается.
Шарон Розенцвейг-Липсон, главный научный сотрудник Life Biosciences, раскрыла планы компании: уже в 2025 году будет подана заявка в FDA на проведение первых клинических испытаний с участием людей.
Суть будущего эксперимента проста, но революционна: пациенты с повреждениями зрения получат инъекции модифицированных факторов Яманаки (без опасного c-Myc), активность которых можно будет регулировать с помощью обычного антибиотика доксициклина. Ученые рассчитывают, что это позволит добиться локального омоложения клеток сетчатки без системного воздействия на организм.
Опухолей быть не должно, так как исключен самый опасный из факторов Яманаки. А гены, судя по животным, не мигрируют из глаз в другие части тела.
Омоложение, но какой ценой?
Сторонники клеточного репрограммирования называют его самым перспективным подходом к увеличению продолжительности и качества жизни. По их словам, эта технология может изменить сам процесс старения. Или даже отменить его.
Однако некоторые исследователи опасаются, что наука движется слишком быстро, и базовые вопросы о безопасности и последствиях клеточного перепрограммирования для людей и общества остаются без ответа.
- Каковы долгосрочные последствия для здоровья?
- Кто получит наибольшую выгоду: богатые спонсоры или любой стареющий или хронически больной человек?
- Сколько это будет стоить?
- И как далеко готовы зайти люди ради возможности продлить жизнь?
«Честно говоря, — говорит Люси Сюй, научный сотрудник Гарвардской медицинской школы, изучающая перепрограммирование на мышах, — эти вопросы не дают мне спать по ночам».
А Чарльз Бреннер, исследователь диабета и рака в калифорнийском исследовательском центре City of Hope, отметил, что перепрограммированные клетки быстро делятся. Прямо как раковые клетки, в которые и могут превратиться.
В масштабном исследовании Стэнфордского университета (март 2024 года) ученые применили частичное репрограммирование либо ко всему телу старых мышей, либо только к их мозгу, надеясь улучшить его состояние.
Но в первом случае в мозге возросло воспаление (по неизвестным причинам) с минимальной пользой для нейронов. Во втором случае появились новые нейроны, но воспаление тоже усилилось, повысив риск нейродегенерации.
Несмотря на это, компания Life Biosciences заявила в своем заявлении, что «остается на верном пути» к скорейшему получению одобрения FDA на клинические испытания репрограммируемой терапии на людях.
Заключение
Клеточное перепрограммирование открывает большие возможности в борьбе со старением. Оно уже доказало свою силу и в экспериментах на животных, и в лабораторных условиях.
А если FDA даст «зеленый свет» компании Life Biosciences, то испытание клеточного перепрограммирования начнется и на людях уже в нынешнем году.
Пока это направление — один из лучших шансов омолодить человеческий организм. Однако ученым предстоит еще многое выяснить, чтобы клеточное перепрограммирование стало безопасным и эффективным.

Статья просто шикарная!