Экспериментальная терапия обещает вернуть вам молодость, вылечить возрастные болезни, возможно, добавить годы жизни. Но мелкий шрифт предупреждает: вместо омоложения вы можете проснуться с зубами, растущими в печени, или с агрессивной опухолью. Готовы ли вы подписать такое согласие?
Это не гипотетический сценарий. Прямо сейчас технология клеточного репрограммирования (или перепрограммирования), которая уже восстановила зрение обезьянам и омолодила органы мышей, готовится к первым испытаниям на людях.
Давайте узнаем, почему одни ученые видят в этой технологии спасение от старости, а другие — биологическую мину замедленного действия.
Мышиная история: как больные прогерией стали вновь молодыми

Для исследователей, стремящихся победить старение, ключевым моментом стал революционный эксперимент 2016 года в Институте Солка (Калифорния).
В нем участвовали мыши, генетически «запрограммированные» на ускоренное старение. У них была модель прогерии, редкого заболевания, заставляющего организм стареть в экстремально быстром темпе. Обычно такие животные живут не дольше семи месяцев, в то время как их здоровые сородичи в лаборатории доживают до двух лет.
Специалисты из Солка применили к мышам вирус, который доставил в их организм четыре гена, способных перестраивать ДНК и фактически возвращать клеткам молодость.
В итоге продолжительность жизни подопытных мышей увеличилась на 30 процентов по сравнению с их обычным сроком. Согласно данным, опубликованным в журнале Cell в 2016 году, мыши не только жили дольше, но и демонстрировали улучшение состояния органов, таких как сердце и кожа.
Этот успех положил начало новой главе в стремлении к продлению жизни. Технологические гиганты и инвесторы, вдохновлённые открытием, начали направлять миллиарды долларов в научные центры, исследующие этот метод, который получил название клеточного перепрограммирования.
Факторы Яманаки очищают «дневник» ДНК

Клеточное перепрограммирование — относительно новая область, начавшаяся с открытия 2006 года. Выяснилось, что всего четыре гена (Oct4, SOX2, KLF4 и c-Myc) могут вернуть даже самую старую клетку в эмбриональное состояние.
Эти гены и их эффекты открыл японский ученый Синъя Яманака из Киотского университета. В 2012 году он получил Нобелевскую премию за свою работу, а гены назвали в его честь — факторы Яманаки.
Работа Яманаки позволяет ученым брать легкодоступные клетки (например, кожу или волосы) и перепрограммировать их. Этот подход аналогичен покупке подержанного ноутбука и очистке жесткого диска перед загрузкой нового программного обеспечения.
Когда факторы Яманаки вводятся в клетку, они быстро «очищают» ДНК от внешнего слоя, известного как эпигеном.
Если вы когда-нибудь задумывались, почему клетки сердца знают, что они должны быть клетками сердца, а не кожи, кишечника или чего-то еще, поблагодарите свой эпигеном. Именно он определяет идентичность каждой клетки.
Одним из важнейших процессов в эпигеноме считается метилирование — когда к участкам ДНК присоединяются маленькие молекулы, называемые метильными группами. Они «включают» или «выключают» гены, позволяя клетке выполнять конкретную функцию.
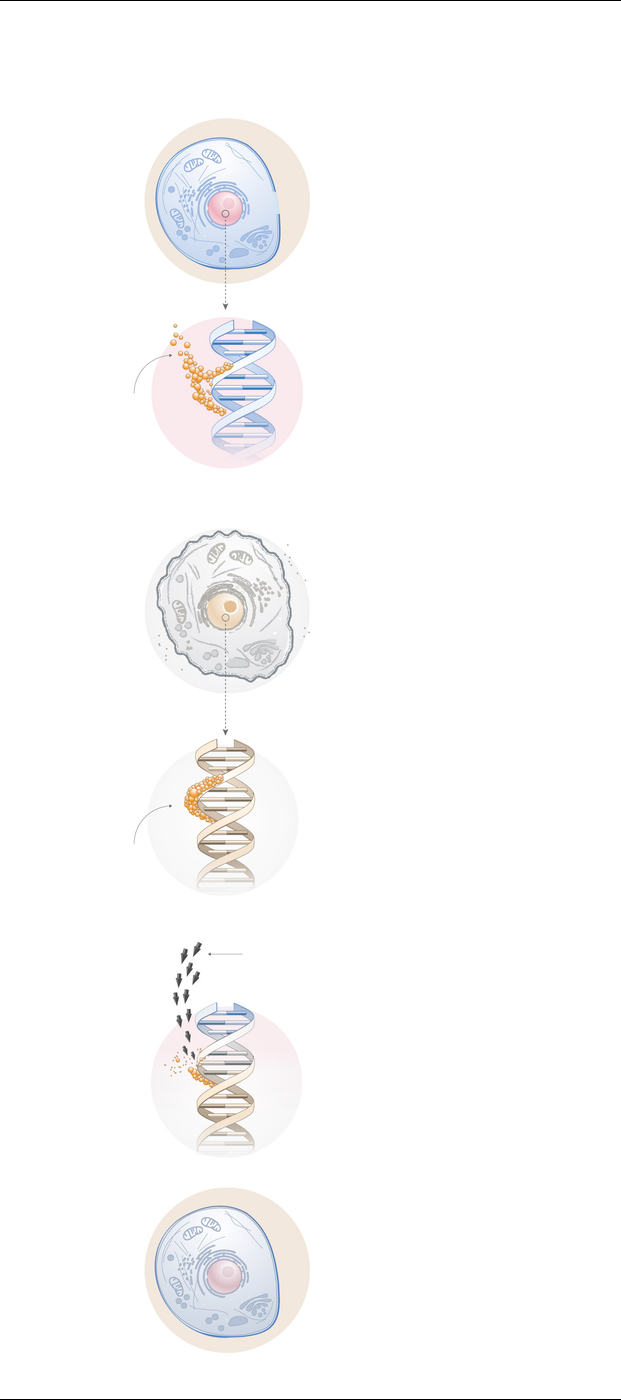
Этот процесс, называемый метилированием, продолжается всю нашу жизнь. На него влияют разные факторы:
- курение,
- физическая активность,
- стресс,
- питание,
- болезни,
- загрязнение воздуха и др.
Благодаря метилированию наш эпигеном является своеобразным дневником тела, где крошечные молекулярные каракули на ДНК записывают, что мы с собой делали.
Но ничто так не влияет на метилирование, как старение. Многие ученые считают, что метилирование не просто фиксирует старение — оно его вызывает.
«Монстрообразные» опухоли
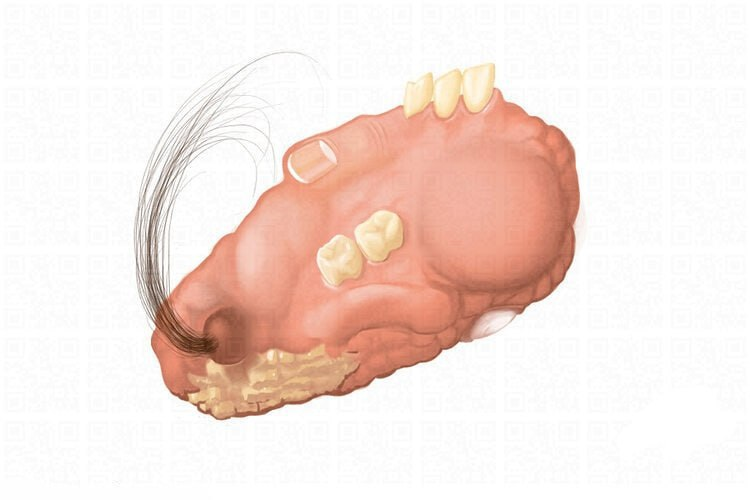
Даже в чашках Петри процесс клеточного перепрограммирования проходит неидеально. Лишь часть клеток послушно превращаются в новорожденные, или, как их называют ученые, плюрипотентные стволовые клетки (iPSC).
Остальные клетки умирают, или — что хуже — превращаются в тератомы: быстрорастущие опухоли, которые могут содержать зубы, кость и другие ткани в неожиданных местах. Например, зуб в тазу или кость в глазу. Хотя такие опухоли редко бывают злокачественными, они вырастают до огромных размеров.
В пробирке тератомы легко удалить. Но в живом организме они становятся настоящим кошмаром. В одном из ранних экспериментов в Испании мыши, на которых испытывали факторы Яманаки, умерли за считанные недели, покрывшись тератомами и другими опухолями.
«У вас всегда будут тератомы во время клеточного перепрограммирования. Это часть процесса», - сказал Пол Нопфлер, профессор Калифорнийского университета в Дэвисе, изучающий эпигенетику, стволовые клетки и рак.
Так что ученые поняли: для того, чтобы использовать клеточное перепрограммирование у людей, нужно сделать его безопаснее.
Продолжение статьи читайте здесь